Giới thiệu
Bản dịch bài báo “Đánh giá hình ảnh học dị dạng động tĩnh mạch não: Bác sĩ lâm sàng cần biết điều gì”. Nội dung trình bày cách tiếp cận thực hành dựa trên hình ảnh khi nghi ngờ tổn thương mạch máu não, bàn luận các đặc điểm khác biệt của nhiều kiểu dị dạng động tĩnh mạch (AVM) và phân biệt những dạng giống AVM với tổn thương thực sự, nêu lên các đặc điểm của AVM não cần phải được đọc kết quả để tạo thuận lợi cho việc đưa ra quyết định theo quan điểm điều trị.
Bản gốc:
– Tiêu đề: Radiologic Assessment of Brain Arteriovenous Malformations: What Clinicians Need to Know
– Tác giả: Sasikhan Geibprasert , Sirintara Pongpech, Pakorn Jiarakongmun, Manohar M. Shroff, Derek C. Armstrong, Timo Krings
– Nguồn: doi.org/10.1148/rg.302095728. Published Online: Mar 8 2010
Bản dịch:
– Tiêu đề: Đánh giá hình ảnh học dị dạng động tĩnh mạch não: Bác sĩ lâm sàng cần biết điều gì
– Người dịch: BS Cao Thiên Tượng / radiocr.vn
Bản song ngữ Anh – Việt:
– [Song ngữ Y khoa] Hình ảnh học dị dạng động tĩnh mạch não
Đánh giá hình ảnh học dị dạng động tĩnh mạch não:
Bác sĩ lâm sàng cần biết điều gì
TÓM TẮT
Dị dạng động tĩnh mạch não (AVM) là các nối kết mạch máu bất thường trong não có lẽ có nguồn gốc bẩm sinh. Có một số phân nhóm, thông thuờng nhất là kiểu AVM não hình cầu, AVM kiểu dò ít gặp hơn. AVM não cũng có thể là một phần của bệnh lý rộng hơn (chẳng hạn như hội chứng phân đọan động tĩnh mạch não-mặt (cerebrofacial arteriovenous metameric syndrome)).Khi gặp phải các mạch máu bệnh lý ở nội sọ trên hình ảnh cắt ngang, cần phải xem xét đến các chẩn đóan khác gồm các bất thường tĩnh mạch bẩm sinh lớn, dò động tĩnh mạch màng cứng ác tính và bệnh moyamoya, vì các nhóm này được biết là có bệnh sử khác biệt và đòi hỏi các lựa chọn điều trị khác nhau. Một số dấu hiệu hình ảnh AVM não có ảnh hưởng đến quyết định xử trí lâm sàng. Điều quan trọng nhất là biết nguy cơ xuất huyết trong tương lai, kể cả bằng chứng xuất huyết trước đó, các túi phình trong ổ dị dạng (nidus), hẹp tĩnh mạch, dẫn lưu tĩnh mạch sâu và vị trí sâu của ổ dị dạng. Các dấu hiệu hình ảnh khác cần phải đưa vào trong kết quả đọc là ảnh hưởng thứ phát do AVM gây ra có thể dẫn đến các khiếm khuyết thần kinh không xuất huyết như xung huyết tĩnh mạch, tăng sinh thần kinh đệm (gliosis), não úng thủy hoặc cướp máu động mạch.
MỞ ĐẦU
Các tổn thương mạch máu não là các tổn thương ít gặp, có thể có khó khăn trong chẩn đóan do các đặc điểm lâm sàng và hình ảnh tương tự. Đã có nhiều hệ thống phân lọai khác nhau. Hệ thống phân lọai thường được sử dụng nhiều nhất là chia các tổn thương mạch máu thành dị dạng động tĩnh mạch (AVM), có thể hoặc là màng mềm hoặc màng cứng phụ thuộc vào vị trí shunt; u mạch hang, dãn mao mạch (capillary telangiectasia) và các bất thường tĩnh mạch bẩm sinh (DVA, trước đây gọi là venous angioma). Tuy nhiên, theo quan điểm lâm sàng, hình ảnh và tiên lượng, cần phân lọai thêm các bệnh lý khác nhau mà trước đây từng được gộp chung thành “AVM não”. Ngòai ra với việc tăng số lượng các AVM được phát hiện tình cờ, nên có lẽ cần xác định thêm khuynh hướng dẫn đến xuất huyết về sau hoặc gây các triệu chứng thần kinh không xuất huyết. Cần nhận ra các bệnh lý giống AVM não để giúp hướng dẫn chẩn đóan và điều trị. Ngòai ra, khi thấy AVM não, cần ghi nhận các chi tiết đặc hiệu liên quan với nguy cơ tự nhiên do AVM và các nguy cơ liên quan với điều trị.
Điểm lưu ý: Nhiều tổn thương mạch máu có thể biểu hiện bất thường mạch máu trong não trên hình ảnh và cần phải phân biệt với nhau do bệnh sử tự nhiên khác nhau và chiến lược điều trị khác nhau. Chẳng hạn, AVM não kinh điển và dò động tĩnh mạch (AVF) màng mềm cần phải xử trí theo nguy cơ liên quan bệnh so với nguy cơ liên quan điều trị, bất thường tĩnh mạch bẩm sinh (DVA) là biến thể bình thường không cần điều trị, và dò động tĩnh mạch màng cứng có dòng trào ngược tĩnh mạch vỏ não luôn cần phải điều trị.
Trong bài này, chúng tôi trình bày một cách tiếp cận thực hành dựa trên hình ảnh khi nghi ngờ tổn thương mạch máu não (hình 1), bàn luận các đặc điểm khác biệt của nhiều kiểu AVM và phân biệt những dạng giống AVM với tổn thương thực sự, nêu lên các đặc điểm của AVM não cần phải được đọc kết quả để tạo thuận lợi cho việc đưa ra quyết định theo quan điểm điều trị.
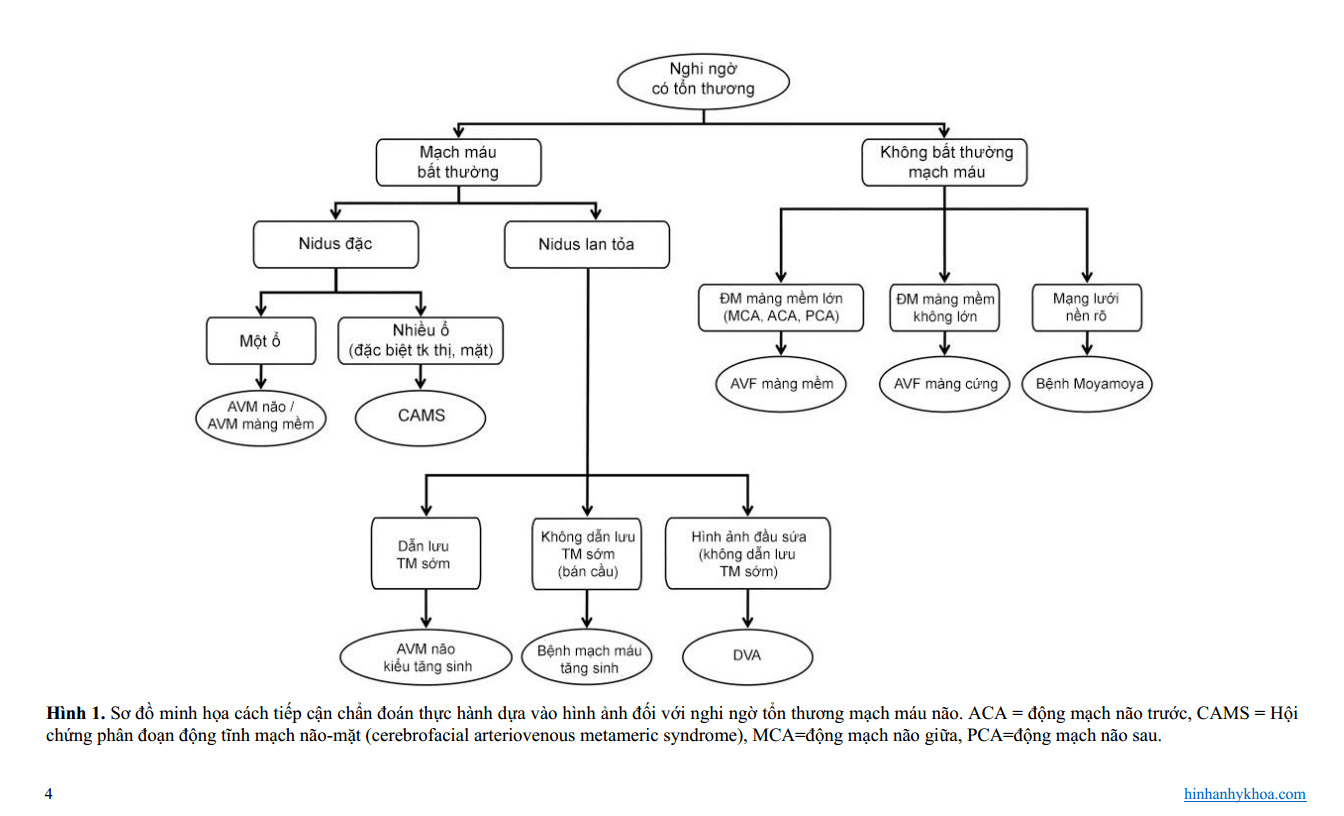
BẤT THƯỜNG MẠCH MÁU TRONG NHU MÔ
AVM não kinh điển
AVM não hoặc AVM màng mềm là các kết nối bất thường giữa các động mạch cấp máu bình thường cho nhu mô não (tức là, mạch máu màng mềm) và các tĩnh mạch dẫn lưu bình thường, dẫn đến shunt động tĩnh mạch với mạng lưới xen kẽ của các mạch máu trong nhu mô não và không có giường mao mạch thực sự. Sự chuyển tiếp giữa động và tĩnh mạch có thể diễn ra thông qua ổ được gọi là nidus (tức là một đám mạch máu bất thường nằm trong nhu mô não) hoặc có thể trực tiếp (tức là dò) mà không có bất kỳ một mạng lưới mạch máu xen kẽ nào. Trong trường hợp sau, người ta dùng thuật ngữ dò động – tĩnh mạch não hay dò động tĩnh mạch màng mềm. Mặc dù AVM não là các tổn thương bẩm sinh, bệnh nhân có xu hướng biểu hiện trễ trong cuộc đời, thường gặp nhất là xuất huyết nội sọ hoặc động kinh.
Điểm lưu ý: Đặc điểm hình ảnh của một AVM não kiểu nidus là hợp với định nghĩa của nó. Tiêu chuẩn chẩn đoán gồm (a) sự hiện diện của một nidus trong nhu mô não, được xác định trên hình ảnh cắt lớp (như CT, MRI) hoặc chụp mạch thường qui; và (b) dẫn lưu tĩnh mạch sớm, thấy rõ nhất trên hình khảo sát dynamic, chuẩn tham chiếu là hình chụp mạch qui ước qua catheter.
Việc lý giải rõ ràng của dẫn lưu tĩnh mạch sớm có thể được đưa ra chỉ nếu tĩnh mạch nhìn thấy ở thì động mạch, điều này cũng nhận ra được trên hình MRA chuẩn hoặc chụp mạch CT nếu như thể tích shunt và tĩnh mạch dẫn lưu đủ lớn. Các phương pháp tạo ảnh như chụp mạch MRI dynamic và chụp mạch CT dynamic ngày càng được dùng để phát hiện dẫn lưu sớm đối với các tổn thương nhỏ hơn và vì vậy dùng trong xác định chẩn đoán, vì các tiêu chuẩn như đã nói trên là quan trọng để phân biệt AVM não với các bệnh mạch máu khác của não.
Nếu có một nidus, có thể gặp hai phân nhóm mạng lưới mạch máu bất thường. Kiểu thông thường là nidus kiểu hình cầu hay kiểu đặc, gồm các mạch máu bất thường mà không có bất kỳ một nhu mô não bình thường nào xen vào (hình 2, 3). Kiểu thứ hai hiếm gặp hơn, còn gọi là nidus kiểu tăng sinh hay lan tỏa, trong đó nhu mô não bình thường xen vào khắp đám rối mạch máu (hình 4). Nếu có dấu hiệu này, bệnh mạch máu tăng sinh hoặc hội chứng phân đoạn động-tĩnh mạch não-mặt (CAMS) cần phải đưa vào trong chẩn đoán phân biệt và có thể phân biệt với AVM não thực sự dựa vào sự vắng mặt của dẫn lưu tĩnh mạch sớm thấy trong bệnh mạch máu tăng sinh, vị trí kinh điển và đi kèm AVM mặt gặp trong CAMS.
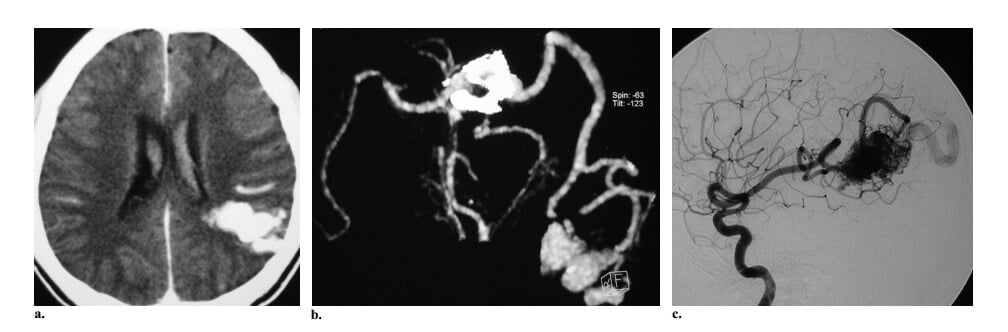
Hình 2: AVM não kiểu nông kinh điển ở bệnh nhân nam 18 tuổi có máu tụ vùng đính trái. (a) Axial cản quang cho thấy một đám rối cấu trúc dạng ống bắt quang mạnh nhúng trong thùy đính trái, một dấu hiệu hợp với nidus. Ghi nhận tăng đậm độ biểu hiện xuất huyết trong não thất. (b) Hình ảnh hướng cường độ tối đa (MIP) (nhì từ đáy) từ dữ liệu chụp mạch CT cho thấy lớn động mạch não giữa trái (so với bên phải), cấp máu cho nidus. (c) Chụp động mạch cảnh trong trái thế nghiêng thấy một nidus kiểu hình cầu ở vị trí vỏ não, được cấp máu chủ yếu bởi nhánh góc và nhánh đính sau của động mạch não giữa trái, với dẫn lưu sớm vào tĩnh mạch vỏ đính trái, các dấu hiệu khẳng định chẩn đoán AVM não.
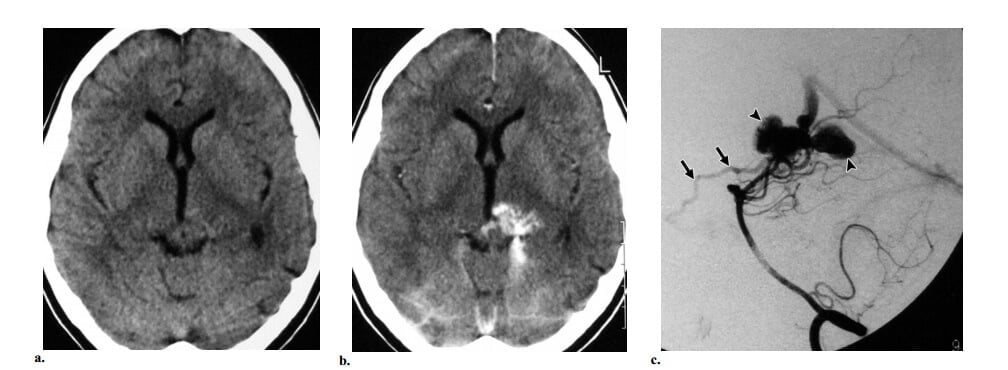
Hình 3: AVM não kiểu sâu kinh điển ở bệnh nhân nữ 19 tuổi đau đầu đột ngột sau đó mất tri giác. Khám thực thể thấy liệt dây thần kinh VI hai bên. (a, b) Axial CT không cản quang (a) và cản quang (b) các cấu trúc mạch máu bắt quang mạnh ở đồi thị trái. Mặt dù không có bằng chứng xuất huyết trên CT, lâm sàng có nghi ngờ hiều đến vỡ. (c) Chụp động mạch cột sống trái thế nghiêng giúp khẳng định sự hiện diện của AVM đồi thị, được cấp máu bởi động mạch xuyên đồi thị và các nhánh động mạch mạch mạc sau trái và dẫn lưu chủ yếu vào tĩnh mạch Galen và dẫn lưu ít vào tĩnh mạch nền của Rosenthal bên trái (mũi tên). Ghi nhận các túi tĩnh mạch nhỏ (đầu mũi tên), sự hiệndiện của các túi này gợi ý nguy cơ xuất huyết cao.
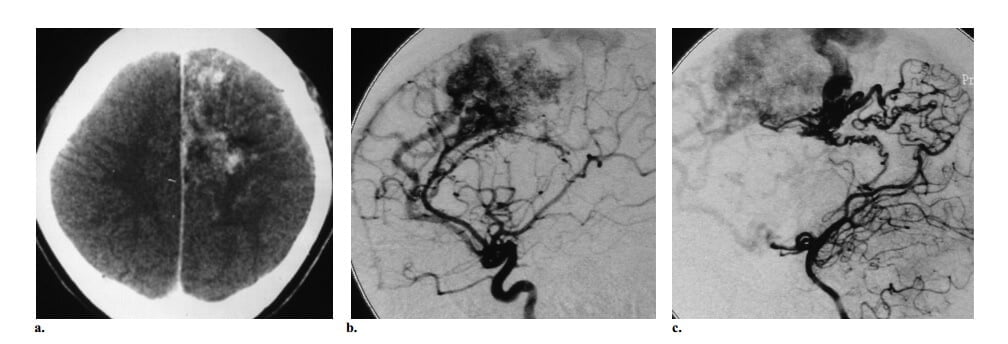
Hình 4: AVM kiểu tăng sinh ở bệnh nhân nữ 27 tuổi có bệnh sử đau đầu 6 năm và động kinh. (a) Axial CT cản quang thấy tổn thương bắt quang mạch máu ở thùy trán cạnh đường dọc giữa trái với vùng đồng đậm độ khu trú bên trong thể hiện nhu mô não bình thường xen kẽ trong nidus. (b, c) Chụp động mạch cảnh trong trái thế nghiêng (b) và động mạch cột sống trái (c) thấy nidus được cấp máu từ các nhánh của cả hai động mạch não trước và nhánh thể chai sau trái, với cấp máu màng mềm từ các nhánh của động mạch não sau trái và dẫn lưu tĩnh mạch sớm vào các tĩnh mạch vỏ não trán cạnh đường dọc giữa, các dấu hiệu khẳng định chẩn đoán AVM. Ghi nhận các vùng thấu quang trong nidus phù hợp với tổn thương kiểu tăng sinh.
Động mạch nuôi và tĩnh mạch dẫn lưu sẽ phụ thuộc vào vị trí của nidus. Các vị trí sâu và não thất sẽ được cấp máu theo thứ tự là các động mạch xuyên (đậu vận, các nhánh xuyên đồi thị) và mạch mạc (các động mạch mạch mạc trước, giữa và sau bên), trong khi dẫn lưu tĩnh mạch thường qua hện thống tĩnh mạch sâu (hình 3). Ở các vị trí nông hơn hoặc vỏ não, cấp máu động mạch chủ yếu là qua các động mạch màng mềm (các nhánh của động mạch não trước, giữa và sau), trong khi tĩnh mạch dẫn lưu chủ yếu qua tĩnh mạch vỏ (hình 2). Không có dẫn lưu tĩnh mạch vỏ trong AVM ở vị trí nông có thể chứng tỏ huyết khối của tĩnh mạch nông đi ra kèm theo là có sự dẫn lưu lại ở hệ thống sâu, điều này có thể gợi ý một tổn thương không ổn định hơn. Cần phải xác định là có hay không có sự cấp máu này nuôi não bình thường (vì kết quả của cướp máu động mạch dẫn đến thiếu máu mạn tính của mô não bình thường được bù trừ bằng sự cấp máu xuyên màng cứng) hoặc sự cấp máu này nuôi bản thân AVM não, xu hướng này thấy trong AVM não kiểu nông kèm khả năng sinh mạch (hoặc tăng sinh).
Hội chứng phân đoạn động tĩnh mạch não-mặt (CAMS)
CAMS (còn được gọi là hội chứng Wyburn- Mason hay bệnh Bonnet-Dechaume-Blanc) là một trong những hội chứng thần kinh mạch máu phân đoạn, là kết quả của đột biến xô ma, xảy ra trong vùng của mào thần kinh hoặc trung bì não kế cận trước khi có sự di trú của các tế bào tiền thể này đến vị trí cuối cùng. Vì các tế bào con mang đột biến “gieo rắc” dọc theo các đường di trú đã được định trước, nên sẽ gặp được các AVM với phân bố phân đoạn (đồng thời, hoặc thường gặp hơn là biến thời).
CAMS kiểu 1 liên quan với phần trong của não trước và sẽ biểu hiện với AVM nằm ở thể chai, hạ đồi (tuyến yên) và mũi. CAM kiểu 2 liên quan với phần ngoài của não trước với AVM ở thùy chẩm và dải thị, bao gồm đồi thị, võng mạc và xương hàm trên (hình 5). CAM kiểu 3 liên quan với trám não và bệnh nhân bị ảnh hưởng sẽ có AVM ở tiểu não, cầu não và xương hàm dưới. Thường gặp sự chồng lên của các lãnh thổ và sẽ dẫn đến kiểu hình hỗn hợp.
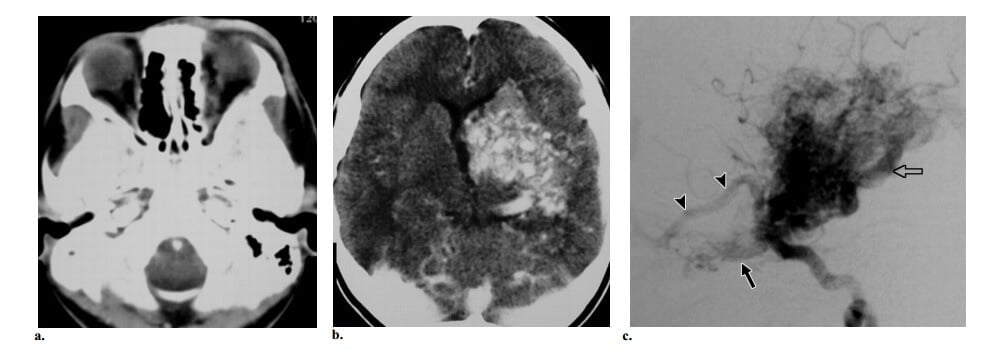
Hình 5: CAMS kiểu 2 ở bé gái 10 tuổi có bệnh sử 1 năm liệt nửa người tiến triển. Ghi nhận phù kết mạc và lồi mắt trái. (a, b) Axial CT ở mức hốc mắt (a) và não (b) thấy tổn thương mạch máu bắt quang ở hạch nền trái. Tổn thương gây hiệu ứng choán chỗ ở não thất bên trái. Ngoài ra, thấy các cấu trúc ngoằn ngoèo xung quanh thần kinh thị. (c) Chụp động mạch cảnh trong thế nghiêng thấy nidus AVM não kiểu tăng sinh ở hạch nền. AVM nhỏ khác được ghi nhận xung quanh thần kinh thị trái (mũi tên đặc). Có dẫn lưu tĩnh mạch sớm ở phía trước vào tĩnh mạch vỏ trán nền (đầu mũi tên) và dẫn lưu ở phía sau vào tĩnh mạch nền của Rosenthal (mũi tên hở).
Manh mối quan trọng nhất để chẩn đoán CAMS là sự hiện diện nhiều AVM ở cả nhu mô não và vùng mặt. AVM não có phân bố đặc trưng như đã nói trên và nidus kiểu tăng sinh hoặc lan tỏa vớ sự cấp máu từ nhiều mạch máu xuyên nhỏ bàng hệ kèm dẫn lưu động tĩnh mạch chậm hơn vào tĩnh mạch, làm cho những AVM này rất khó điều trị. Nếu AVM não có các đặc điểm này trên chụp mạch não thường quy, cần phải tiêm thuốc cản quang vào động mạch cảnh ngoài để giúp đánh giá các dị dạng mạch máu có thể có ở thần kinh thị, hàm mặt hoặc vùng hàm dưới.
Bệnh sử tự nhiên của AVM liên quan với CAMS có lẽ khác với AVM não kinh điển là hiếm khi có biểu hiện xuất huyết. Tuy nhiên, các triệu chứng thần kinh có thể phát sinh thông qua cơ chế bệnh học như não úng thủy tắc nghẽn do các tĩnh mạch dẫn lưu hoặc nidus của AVM, động kinh do xung huyết tĩnh mạch từ huyết khối tiến triển của dẫn lưu tĩnh mạch trong AVM não, và khiếm khuyết thần kinh tiến triển do bản thân AVM não lớn theo thời gian. Thông thường hơn, bệnh nhân sẽ có triệu chứng liên quan với AVM mặt gồm giảm thị lực tiến triển dẫn đến mù, chảy máu răng và lợi, và vấn đềthẩm mỹ (chẳng hạn, bất đối xứng mặt). Chảy máu tái phát từ AVM hàm trên và hàm dưới thường nặng, và điều trị nội mạch là lực chọn tốt nhất trong trường hợp cấp cứu (hình 6). Tuy nhiên, phẫu thuật cắt bỏ (nếu được) vẫn còn là phương pháp điều trị chọn lựa cho AVM mặt.
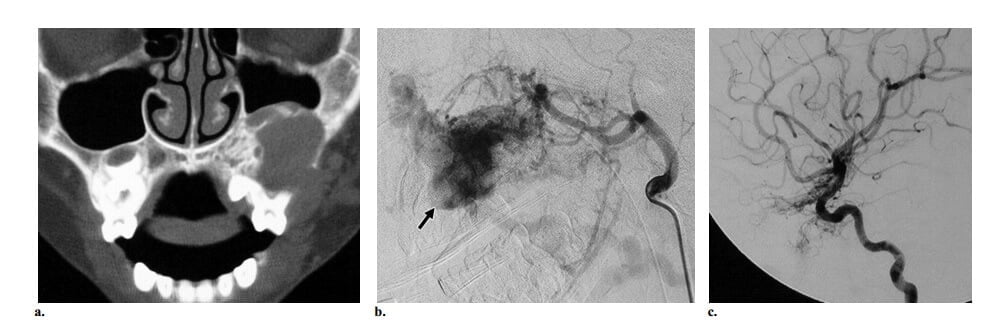
Hình 6: CAMS type 2 ở bé gái 7 tuổi có từng đợt chảy máu lợi tái phát do mọc răng hàm trái. (a) Coronal CT (cửa sổ xương) thấy tổn thương hủy xương trong cầu ổ răng của xương hàm trên trái. (b, c) Chụp động mạch cảnh ngoài (b) và động mạch cảnh trong (c) thấy AVM xương mặt được cấp máu bởi các nhánh hàm trong và động mạch mặt ngang, dẫn lưu về túi tĩnh mạch trong xương (mũi tên ở b). Dấu hiệu này tương ứng với tổn thương hủy xương thấy ở a và được chứng minh là nguồn chảy máu của bệnh nhân. Cũng ghi nhận một AVM thần kinh thị trái, vì vậy cho phép chẩn đáon AMS type 2 Trong trường hợp này, thuyên tắc mạch cấp cứu của AVM mặt được thực hiện để làm ngừng chảy máu.
Bệnh mạch máu tăng sinh
Bệnh mạch máu não tăng sinh, trước đây được gọi là AVM kiểu nidus lan tỏa, chiếm khoảng 2-4 % toàn bộ các AVM não. Người ta cho rằng nó là một nhóm tách biệt với AVM não kinh điển. Nữ chiếm ưu thế với tỉ lệ 2:1, tuổi trung bình trẻ hơn (20 tuổi). Khiếm khuyết thần kinh tiến triển, cơn thiếu máu thoáng qua, động kinh, đau đầu là các triệu chứng thường gặp, còn xuất huyết rất hiếm gặp. Mặc dầu chưa rõ bệnh nguyên, bệnh có đặc điểm là tăng sinh nội mạc và sinh mạch. “Nidus” gồm nhiều động mạch vì đáp ứng sinh mạch đối với thiếu máu vỏ não.
Các dấu hiệu CT và MRI điển hình gồm nidus kiểu tăng sinh, trong đó nhu mô não bình thường nằm xen kẽ giữa các mạch máu bất thường. Thông thường, toàn bộ một thùy não hoặc toàn bộ bán cầu não bị ảnh hưởng (hình 7). Trên hình chụp mạch não, động mạch nuôi có xu hướng kích thước bình thường hoặc chỉ lớn vừa phải. Thường thấy hẹp các mạch máu nuôi đi kèm và có sự cấp máu xuyên màng cứng phong phú đối với nhu mô não bình thường và bất thường thông qua các nhánh của động mạch cảnh ngoài. Không có dẫn lưu tĩnh mạch sớm rõ rệt trên hình dynamic là điểm mấu chốt để chẩn đoán phân biệt bệnh này với AVM não kinh điển. Vì cơ chế bệnh học của bệnh mạch máu tăng sinh chủ yếu do thiếu máu vỏ não (được chứng minh trên các nghiên cứu hình ảnh tưới máu), đã có các báo các về điều trị thành công bằng cách kết nối đồng thời nhiều mạch máu màng mềm (pial synangiosis) hoặc tạo lỗ thông ở sọ để tăng cường cấp máu cho mô não khỏe mạnh từ động mạch cảnh ngoài.
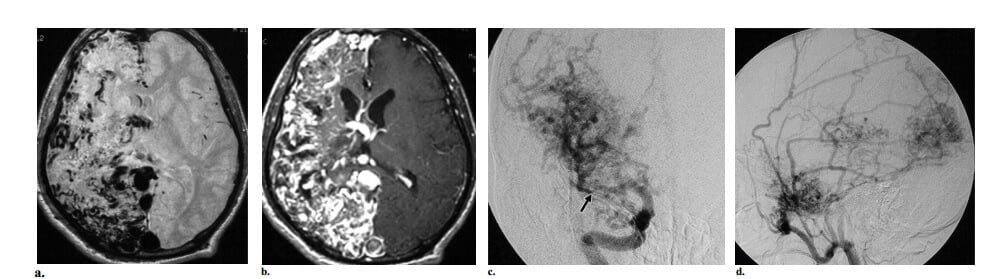
Hình 7: Bệnh mạch máu tăng sinh ở bệnh nhân nam 26 tuổi bị yếu 1/2 người trái tiến triển. (a,b) Axial PD (a) và T1W có Gd (b) cho thấy nhiều cấu trúc tín hiệu trống và bắt thuốc dạng ống biểu hiện tổn thương mạch máu lớn liên quan với toàn bộ bán cầu não phải. Nhu mô não bình thường len giữa các mạch máu bất thường. (c) Chụp động mạch cảnh trong thế trước sau thấy các nhánh động mạch não giữa kích thước tương đối bình thường và không có tĩnh mạch dẫn lưu sớm, các dấu hiệu này khẳng định chẩn đoán bệnh mạch máu tăng sinh. Hẹp đoạn gần M2 của động mạch cảnh trong phải xa với chỗ phân nhánh động mạch cảnh trong (mũi tên). (d) Chụp động mạch cảnh ngoài phải thế nghiêng cho thấy cấp máu xuyên màng cứng phong phú ở bán cầu não phải thông qua các nhánh của động mạch màng não giữa. Cũng có liên quan với động mạch não sau trái (không chỉ ra).
Các bất thường tĩnh mạch bẩm sinh (DVA)
Mặc dù không được phân loại như AVM, các DVA có thể biểu hiện trên hình ảnh cắt lớp với một búi các mạch máu trong nhu mô và là một biến thể cực biên của hệ thống tĩnh mạch xuyên não bình thường. Mặc dù DVA không có triệu chúng trong hầu hết các trường hợp, chúng có thể có triệu chứng với thiếu máu hoặc nhồi máu tĩnh mạch nếu dòng ra của các tĩnh mạch góp bị tổn thương. DVA được cho là đáp ứng ngẫu nhiên xảy ra trong thời kỳ sinh phôi giữa giai đoạn thứ tư đến thứ bảy của phát triển phôi (tức là, trong khoảng chiều dài 40- 80mm) như đã được mô tả bởi nhà mô hộc thần kinh D. H. Padget trong một nghiên cứu vào năm 1948, dẫn đến tắc nghẽn hoặc kém phát triển của các tĩnh mạch nông hoặc sâu. Do tính mềm dẻo của hệ thống mạch máu ở giai đoạn này, DVA được hình thành như là các đường bù trừ, phục hồi và dãn các tĩnh mạch xuyên tủy tồn tại trước đó.
Trên CT và MRI các tĩnh mạch góp có thể thấy như là cấu trúc bắt thuốc dạng đường thẳng hoặc đường cong, hoặc tín hiệu trống. Cũng có thể quan sát thấy bắt thuốc các tĩnh mạch tủy dãn (hình ảnh “đầu sứa”). Các DVA lớn có thể dễ phân biệt với AVM não trên hình chụp mạch. Đặc điểm hình ảnh chụp mạc điển hình là “đầu sứa” (hoặc hình ảnh “chiếc dù ngược”) của các tĩnh mạch xuyên tủy (chỉ thấy ở thì tĩnh mạch) dẫn lưu về tĩnh mạch góp, tĩnh mạch này tiếp tục dẫn lưu về hệ thống tĩnh mạch nông hoặc sâu. Một sự đổi màu mao quản dày đặc có thể thấy ở các tổn thương lớn, tuy nhiên, không có lớn động mạch gợi ý DVA. Trong các trường hợp ngoại lệ, các tĩnh mạch của đầu sứa có thể thấy sớm hơn (tức là, ở thì mao mạch trễ) do thời gian chuyển tiếp mao mạch nhanh hơn nhờ việc dãn các khoang mao mạch, một dấu hiệu không được phép đọc nhầm với shunt động-tĩnh mạch.
Điểm chú ý: Vì DVA hiếm khi gây chảy máu, nên nếu một DVA gặp trong khi khảo sát là nguyên nhân xuất huyết nội sọ, cần phải tìm kiếm u mạch hang đi kèm vả có thể thấy rõ nhất ở chuỗi xung GRE hoặc chuỗ xung phụ thuộc nồng độ oxygen máu.
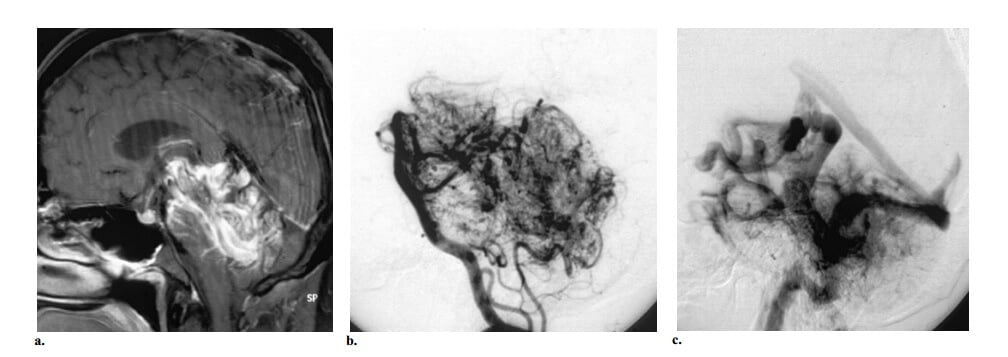
Hình 8: DVA ở bệnh nhân nam 25 tuổi đau đầu và tổn thương mạch máu phát hiện tình cờ. (a) Hình MRI sagittal T1W Gd thấy nhiều cấu trúc dạng ống bắt thuốc, chủ yếu ở trong thân não và thùy giun, với nhu mô não bình thường len vào. Một số DVA có hình ảnh đầu sứa, nhưng vì kích thước lớn nên tổn thương trong trường hợp này khó phân biệt với AVM não chỉ dựa đơn thuần vào dấu hiệu MRI. (b, c) Hình chụp mạch cột sống trái thì động mạch trên thế ghiêng (b) và thì tĩnh mạch (c) thấy tẩm nhuận mao mạch dày đặc trong thân não và thùy giun; tuy nhiên, không có lớn động mạch hoặc dẫn lưu tĩnh mạch sớm. Hình ảnh đầu sứa của tĩnh mạch xuyên tủy dẫn lưu vào nhiều tĩnh mạch góp thấy rõ ở thì tĩnh mạch.
BẤT THƯỜNG MẠCH MÁU NGOÀI NHU MÔ
AVF màng mềm
Mặc dù thuộc về nhóm AVM màng mềm “thực sự” , AVF màng mềm không thấy đám rối mạch máu trong nhu mô kinh điển. AVF màng mềm là một phân nhóm đặc biệt của shunt động – tĩnh mạch não và chiếm khoảng 5% các AVM não. Chúng tạo thành shunt động tĩnh mạch thực sự và gồm một thong nối dò trực tiếp giữa động và tĩnh mạch màng mềm mà không có nidus xen vào. AVF màng mềm nằm ở bề mặt não, là tổn thương thường có dòng chảy ca, và trong hầu hết các trường hợp có liên quan với túi tĩnh mạch dãn. AVF màng mềm thường gặp ở trẻ em và thường liên quan với dãn mao mạch xa (telangiectasia) xuất huyết di truyền.
Manh mối để chẩn đoán AVF màng mềm trên hình ảnh cắt lớp gồm sự hiện diện của (a) các mạch máu dãn, chủ yếu ở bề mặt não; và (b) dãn bất đối xứng của động mạch nuôi màng mềm – hoặc là động mạch não giữa, não trước hoặc não sau- thường thấy rõ nhất ở vòng Willis. Các dấu hiệu này có thể dùng để phân biệt AVF màng mềm với AVF màng cứng (hình 9) và có thể đi kèm với túi tĩnh mạch dãn ở bên ngoài nhu mô não.
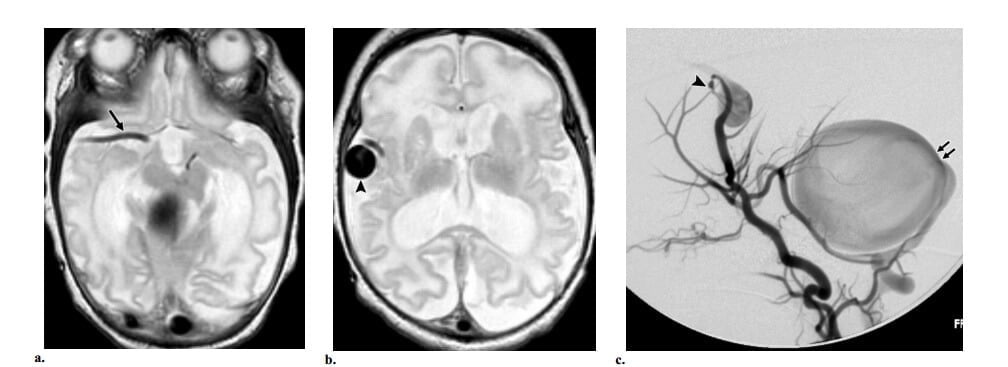
Hình 9: AVF màng mềm ở trẻ sơ sinh 1 tuần tuổi bị suy tim xung huyết. Bệnh nhân có bệnh sử gia đình dãn mao mạch xa xuất huyết di truyền. (a, b) Axial MRI T2W thấy lớn động mạch não giữa phải ở ngang mức vòng Willis (mũi tên ở a) và một cấu trúc mạch máu dãn lớn ở vùng quanh rãnh sylvien phải (đầu mũi tên ở b), dấu hiệu gợi ý túi tĩnh mạch. Phần trên của cấu trúc flow void lớn khác cũn g nhìn thấy ở hố sau. (c)Chụp động mạch cảnh trong phải thế nghiêng thấy dò dòng chảy cao giữa nhánh động mạch não giữa và túi tĩnh mạch lớn (đầu mũi tên). Dòng ngược chiều của thuốc cản quang đi vào động mạch thân nền khẳng định sự hiện diện của dò dòng chảy cao khác (mũi tên) từ động mạch tiểu não sau dưới. Dò dòng chảy cao và túi tĩnh mạch là các dấu hiệu điển hình ở bệnh nhân bị dãn mao mạch xa xuất huyết di truyền.
AVF màng cứng
AVM màng cứng là các kết nối bất thường giữa các động mạch có thể nuôi một cách bình thường màng não, xương hoặc cơ nhưng không phải cho não, và các tiểu tĩnh mạch nhỏ trong màng cứng. Chúng chiếm 10-15% tất cả các shunt động tĩnh mạch nội sọ. Các đơn giản nhất để phân loại các tổn thương này là nhóm chúng thành nhóm có hay không có dòng hồi lưu tĩnh mạch vỏ. Nhóm không có hồi lưu tĩnh mạch là dò lành tính (Borden kiểu 1) hầu như không bao giờ dẫn đến khiếm khuyết thần kinh, còn nhóm có hồi lưu tĩnh mạch vỏ là dò ác tính (Borden kiểu 2 và 3). Dò động tĩnh mạch màng cứng ác tính thường có diễn tiến lâm sàng nặng, bao gồm xuất huyết nội sọ, động kinh, sa sút trí tuệ, thay đổi tri giác và các triệu chứng thần kinh khu trú không xuất huyết do xung huyết tĩnh mạch hoặc vỡ túi tĩnh mạch.
AVF màng cứng có hồi lưu tĩnh mạch vỏ sẽ có biểu hiện mạch máu bất thường ngoài nhu mô não và cần phải phân biệt với các shunt mạch máu khác.
Điểm lưu ý: Các dấu hiệu CT và MRI gồm dãn tĩnh mạch vỏ não (một tình trạng được xem như là dạng giả viêm tĩnh mạch theo một số tác giả), có biểu hiện là các trúc dạng ống bắt thuốc bất thường hoặc flow void trong các rãnh vỏ não kèm không có nidus thực sự trong nhu mô não (hình 10).
Giảm đậm độ chất trắng trên CT hoặc tăng tín hiệu T2W trên MRI chứng tỏ xung huyết tĩnh mạch hoặc nhồi máu, cuối cùng có thể dẫn đến xuất huyết tĩnh mạch. Bắt quang khu trú các vùng nảy cũng có thể được quan sát thấy là một dấu hiệu của thiếu máu tĩnh mạch mạn tính. Đóng vôi dưới vỏ dạng đường cong có thể thấy trên CT ở bệnh nhân có hồi lưu tĩnh mạch vỏ não kéo dài, có thể do xung huyết tĩnh mạch mạn tính. Tuy nhiên, hình ảnh cắt lớp đơn độc thường không đủ để định vị AVF màng cứng. Các khảo sát động với MRA , CTA hoặc DSA (tham chiếu chuẩn) sẽ cho thấy lấp đầy tĩnh mạch sớm, sự đóng góp của các nhánh động mạch cảnh ngoài (hơn là các mạch máu màng mêm) và vị trí shunt. Bắt buộc phải điều trị cho AVF màng cứng do diễn tiến tự nhiên kém nếu không điều trị.
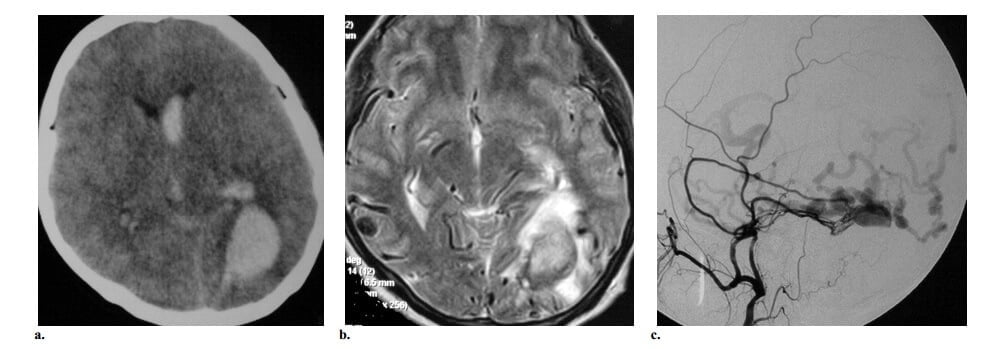
Hình 10: AVF màng cứng Borden type 2 ở phụ nữ 45 tuổi bị mất tri giác đột ngột. (a) Axial CT không cản quang thấy máu tụ thái dương chẩm trái với xuất huyết trong não thất. (b) Axial T2w cho thấy nhiều cấu trúc fliod voids mạch máu dọc theo các rãnh vỏ não của vùng chẩm hai bên. Có phù chất trắng với tăng tín hiệu trên T2W ở thùy chẩm trái. Không thấy nidus. (c) Chụp động mạch hàm trong trái cho thấy AVF màng cứng ở xoang ngang trái được cấp máu bởi động mạch màng não giữa trái. Ghi nhận có huyết khối đi kèm của phần gần và phần xa xoang ngang, tạo thành một “túi riêng biệt” và vì vậy gây ra dòng ngược từ shunt vào các tĩnh mạch vỏ não.
Bệnh Moyamoya
Bệnh moyamoya (tiếng nhật nghĩa là “khói thuốc lá”) là một bệnh lý tắc nghẽn ít gắp có nguồn gốc không rõ, về mặt kinh điển liên quan với các động mạch cảnh trong trên mấu giường yên, hố sau tương đối bình thường ở giai đoạn sớm. Thuật ngữ hội chứng moyamoya được dùng trong các trường hợp không thể xác định được nguyên nhân gốc (xơ vữa độngmạch, hội chứng Down, bệnh đa u sợi thần kinh, bệnh hồng cầu hình liềm hoặc một số bệnh khác). Thường có sự phát sinh rất nhiều mạch máu bàng hệ ở các nhánh xuyên vùng nền (các mạch máu moyamoya), đã được mô tả là hình ảnh khói thuốc lá trên hìnhchụp mạch máu não và các mạch máu bàng hệ xuyên màng cứng. Biểu hiện lâm sàng khác nhau giữa hai nhóm trẻ em và người lớn: hầu hết trẻ em có cơn thiếu máu thoáng qua hoặc nhồi máu não trong khi có một nửa số người lớn có xuất huyết nội sọ do vỡ các mạch máu bàng hệ moyamoya.
Manh mối hình ảnh học trên CT và MRI gồm sự hiện diện của nhiều tín hiệu flow voids thường thấy xuất phát từ bể nền và lan vào hạch nền hoặc đồi thị. Không có nidus thực sự nằm trong nhu mô não và không có dãn mạch máu (hình 11). Mặc dầu chẩn đoán có thể gợi ý bằng sự hiện diện của hẹp động mạch cảnh trong trên mấu giường yên hai bên trên hình chụp mạch CT và MR, nhưng chụp mạch máu vẫn còn cần thiết để đánh giá trước phẫu thuật cho việc tái tạo mạch máu của bệnh moyamoya. Tập hợp các đường bàng hệ thứ phát (các mạch máu bàng hệ moyamoya nhánh xuyên hạch nền, cấp máu xuyên màng cứng từ động mạch màng não giữa đến lối não và thông qua động mạch mắt đến các nhánh động mạch não trước) thường có thể được đánh giá chỉ bằng chụp DSA do kích thước nhỏ. Các nghiên cứu mới đây đã chứng minh rằng hình ảnh MR tưới máu và các khảo sát bảo tồn mạch máu não có thể chọn lựa trước phẫu thuật và theo dõi sau phẫu thuật sau khi phẫu thuật tái tạo mạch máu.
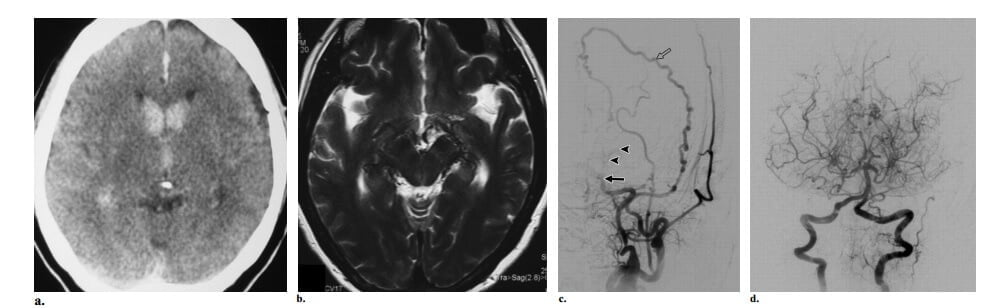
Hình 11: Bệnh moyamoya ở nữ 28 tuổi trải qua hai đợt xuất huyết nội sọ tái phát. (a) Axial CT cho thấy xuất huyết trong não thất. (b) Axial T2W thấy rất nhiều flow voids trong bể quanh gian não và quanh não giữa. Không thấy nidus. (c) Hình chụp động mạch cảnh trong thế trước sau thấy tắc động mạch cảnh trong trên mấu giường yên (mũi tên đặc) với rất nhiều mạch máu bàng hệ nhánh xuyên (đầu mũi tên). Cùng ghi nhận có cấp máu bàng hệ xuyên màng cứng từ động mạch màng não giữa (mũi tên hở). (d). Chụp động mạch cột sống trước sau cho thấy có liên quan các động mạch não sau, cùng với việc không có mạch máu bàng hệ hình khói thuốc lá gợi ý bệnh ở giai đoạn sau.
ĐÁNH GIÁ VÀ ĐIỀU TRỊ CÁC AVM NÃO
Hình ảnh AVM não: các bác sĩ lâm sang cần biết điều gì
Sau khi đưa ra chẩn đoán AVM não thực sự, cần phải trả lời một số câu hỏi liên quan với các nguy cơ khiếm khuyết thần kinh biết trước (cả xuất huyết và không xuất huyết) và các yếu tố báo trước liên quan với điều trị. Trong số các biến chứng liên quan với AVM não xuất huyết nội sọ là đáng sợ nhất. Vì vậy, nhiều nghiên cứu khác nhau đã tỉm cách xác định các yếu tồ liên quan với nguy cơ cao xuất huyết trong tương lai. Các đặc điểm được tóm tắt ở bảng 1 đã xác định các nguy cơ liên quan của xuất huyết và khiếm khuyết thần kinh trong tương lai, và các yếu tố đó quan trọng mà bác sĩ lâm sàng cần biết.

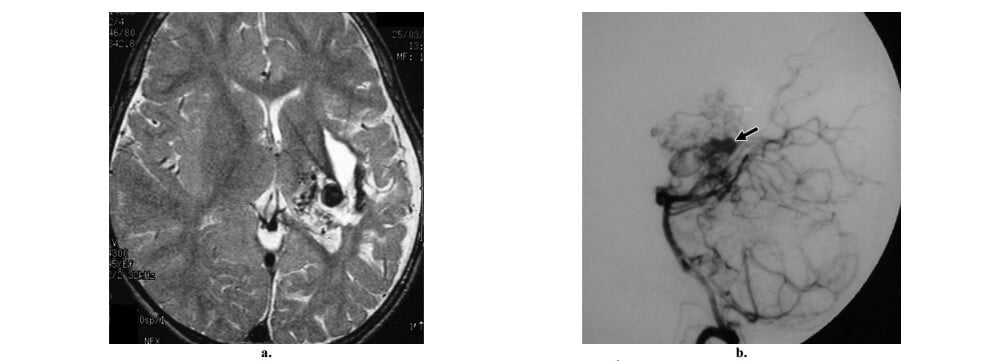
Hình 12: AVM đồi thị Spetzler-Martin độ 3 có phình mạch trong nidus ở bé gái 4 tuổi xuất huyết nội sọ tái đi tái lại. (a) Axial T2W thấy một đám mạch máu bất thường ở đồi thị trái, tương ứng với nidus. Có vùng xung quanh tăng tín hiệu trên T2W với viền tín hiệu thấp, dấu hiệu gợi ý xuất huyết trước đây. Cũng ghi nhận cấu trúc flow void tròn ở phía sau bên của nidus, khả năng là một phình mạch trong nidus. (b) Hình chụp động mạch cột sống trái nghiêng cho thấy cấp máu đến nidus AVM từ các mạch máu xuyên đồi thị và động mạch mạch mạc sau trái. Ghi nhận lấp đầy thuốc cản quang sớm của một phình mạch nhỏ trong nidus (mũi tên).
Ở các bệnh nhân AVM não có chảy máu cấp, dấu hiệu quan trọng nhất cần liên lạc khẩn với bác sĩ lâm sàng (ngoài các dấu hiệu đe dọa tính mạng như đẩy đường giữa hoặc thoát vị) là sự hiện diện của phình mạch trong nidus hoặc túi tĩnh mạch (hình 3, 12) do nguy cơ cao xuất huyết tái phát sớm.
Vì xuất huyết trước đây là yếu tố dự báo chắc chắn và quan trọng nhất của xuất huyết trong tương lai, trong trường hợp AVM não được phát hiện tình cờ, trước hết cần phải phân biệt AVM não có chảy máu với AVM não không chảy máu, mà trong hầu hết các trường hợp có thể xem lại bệnh sử lâm sàng. Chuỗi xung GRE T2W nhạy cao trong việc mô tả các dấu hiệu xuất huyết cũ, có thể giúp nhận ra được xuất huyết dưới lâm sang ở những bệnh nhân không có triệu chứng nhưng cực kỳ hiếm.
Điểm lưu ý: Ngoài ra, cầu phải đưa vào trong kết quả đọc các điểm yếu về cấu trúc mạch đặc hiệu, vì chúng có thể làm tăng nguy cơ xuất huyết trong tương lai. Phình mạch trong nidus, túi dãn tĩnh mạch, hẹp tĩnh mạch, dẫn lưu tĩnh mạch sâu, chỉ dẫn lưu một tĩnh mạch và vị trí hố sau hợp thành các điểm yếu cấu trúc mạch.
Tuổi cao và phái nam cũng có thể làm tăng nguy cơ xuất huyết. Mặc dù nguyên tắc này không được chứng minh trong các nghiên cứu tiền cứu ngẫu nhiên, chúng tôi đã sử dụng nó trên thực tế lâm sàng trong 20 năm qua và có thể đã cho thấy kết quả cải thiện trên những trường hợp theo dõi so với diễn tiến tự nhiên.
Tuy nhiên, điều trị có thể được chỉ định trong AVM không chảy máu và không cho thấy các điểm yếu cấu trúc mạch. Trong số đó, shunt dòng chảy cao có thể dẫn đến chậm phát triển tâm thần vận động và suy tim ở trẻ em, khi hiện diện ở người lớn có thể dẫn đến sa sút trí tuệ và vì vậy có chỉ định điều trị với mục đích làm giảm thể tích shunt động tĩnh mạch. Xung huyết tĩnh mạch do dòng vào cao (tổn thương dò) (hình 13) hoặc giảm dòng ra (hẹp thứ phát của dạng dòng ra ) có thể liên quan với suy giảm nhận thức hoặc động kinh; vì vậy, điều trị hướng đến việc làm giảm thể tích shunt động tĩnh mạch là cần thiết. Ngay cả nếu không có các dấu hiệu xung huyết tĩnh mạch, đường đi tĩnh mạch dẫn lưu màng mềm dài có thể chỉ ra rằng hạn chế dẫn lưu tĩnh mạch hiện diện qua một vùng lớn, làm tăng nguy cơ xung huyết tĩnh mạch và dẫn đến động kinh. Ngược lại, tĩnh mạch ngắn hầu như luôn luôn dẫn lưu trực tiếp vào xoang màng cứng có lẽ không ảnh hưởng đến dẫn lưu não bình thường. Nếu bệnh nhân có loại cấu trúc mạch này mà cũng có động kinh, thì hình ảnh MRI cẩn phải xem xét đến tăng sinh thần kinh đệm xung quanh nidus. Trong trường hợp đầu (bệnh nhân động kinh có AVM với tĩnh mạch dẫn lưu màng mềm dài), việc điều trị nội mạch bảo đảm để làm giảm sự cản trở dẫn lưu não bình thường và có lẽ để làm giảm tần số hoặc độ nặng động kinh; trong trường hợp sau (động kinh sau khi có tăng sinh thần kinh đệm quanh nidus), điều trị nội mạch có lẽ không làm thay đổi tần số và độ nặng của động kinh. Hiệu ứng choán chỗ là một cơ chế bệnh học hiếm gặp, có thể do dãn các tĩnh mạch lớn hoặc chèn ép các cấu trúc quan trọng bởi nidus và có thể dẫn đến động kinh, khiếm khuyết thần kinh và thậm chí não úng thủy. Cướp máu động mạch liên quan với các dấu hiệu lâm sàng (chẳng hạn, migraine và các triệu chứng thần kinh khu trú), thường chỉ có tính chất thoáng qua. Với sự đạt được của các phương pháp hình ảnh mới như MRI chức năng và hình ảnh tưới máu, hiện nay có thể xác định được các triệu chứng có thể được cho là do cướp máu thực sự hay không, điều đó có thể được điều trị bằng nội mạch với mục tiêu làm giảm thể tích shunt nếu triệu chứng không giảm.
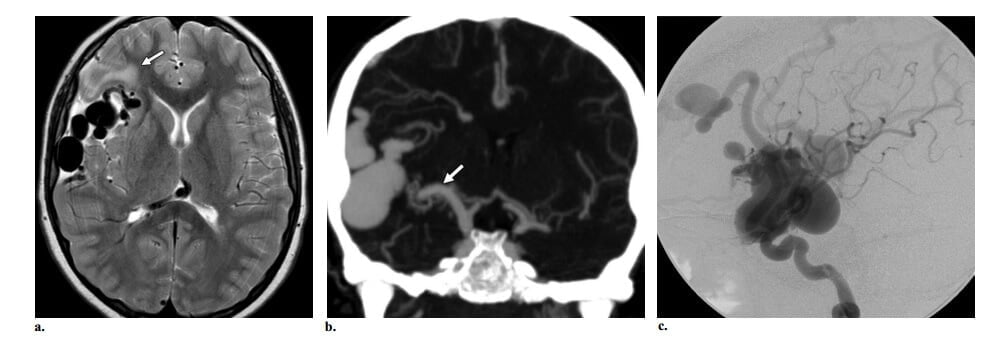
Hình 13: AVF màng mềm có các túi tĩnh mạch và xung huyết tĩnh mạch ở bé trai 7 tuổi bị đau đầu. Bệnh nhân có bệnh sử gia đình chảy máu mũi và giãn mao mạch ở niêm mạc gợi ý dãn mao mạch xuất huyết di truyền. (a, b) Axial T2W (a) và chụp mạch Coronal CT (b) thấy cấu trúc mạch máu dãn, lớn trong vùng quanh rãnh sylvien hải gợi ý túi tĩnh mạch kèm lớn động mạch não giữa phải so với bên trái (mũi tên ở b) và không thấy nidus, các dấu hiệu phù hợp với AVF màng mềm. Tăng tín hiệu trên T2W ở chất trắng thùy trán phải (mũi tên ở a) gợi ý xung huyết tĩnh mạch. (c) Hình chụp động mạch cảnh trong thế nghiêng thấy dò dòng chảy cao giữa nhánh động mạch não giữa và các túi tĩnh mạch lớn.
Chọn lựa điều trị
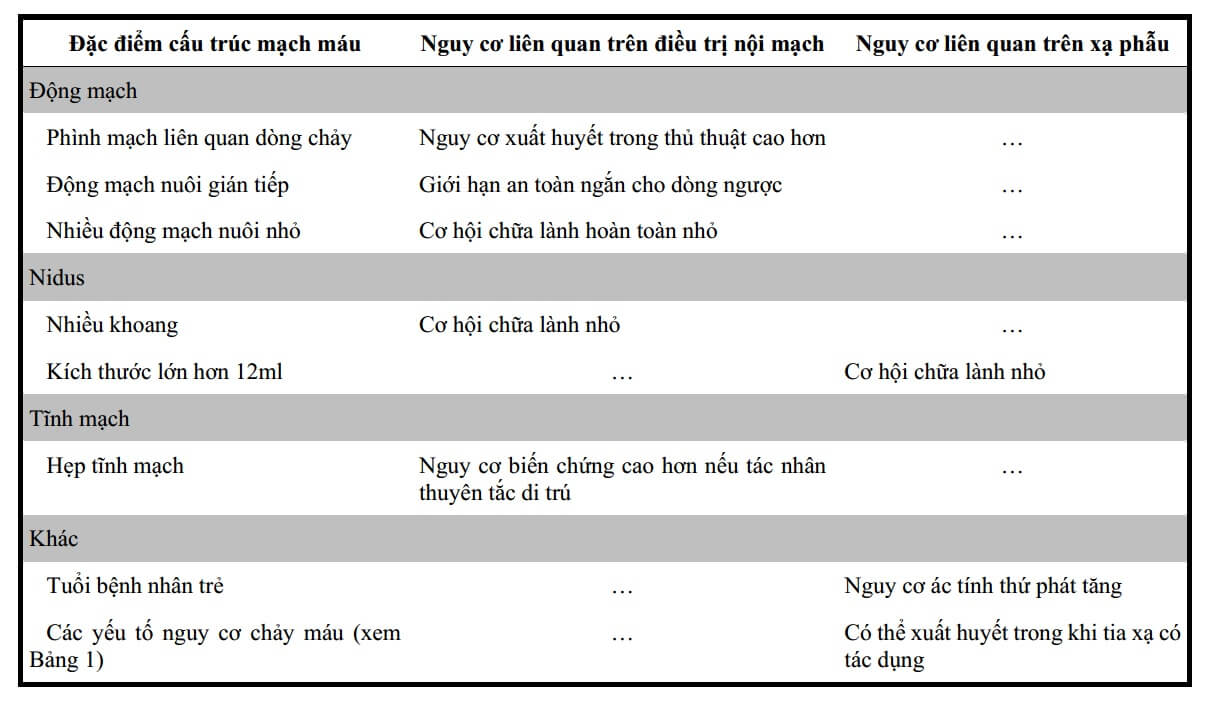
Ngoài việc xử trí bảo tồn, có ba chọn lựa điều trị cho AVM não: phẫu thuật, thuyên tắc nội mạch và xạ phẫu. Mỗi phương pháp có độ mạnh và giới hạn riêng và tiếp cận đa mô thức thường được sử dụng nhất. Có một số đặc điểm hình ảnh và lâm sàng quan trọng trong việc quyết định phương pháp điều trị hiệu quả nhất và an toàn nhất. Phẫu thuật có thể chữa khỏi nhanh trong các trường hợp thích hợp; tuy nhiên, tỉ lệ biến chứng phụ thuộc phần lớn vào độ Spetzler- Martin: độ càng cao (hoặc thấp) thì tỉ lệ biến chứng càng cao (hoặc thấp). Vì vậy, các bệnh nhân có AVM não nhỏ hơn có lẽ tốt nhất là phẫu thuật cắt bỏ (hình14). Thuyên tắc nội mạch là một lựa chọn điều trị khác có thể dùng để loại bỏ nhanh các yếu tố nguy cơ trên chụp mạch máu. Không có chống chỉ định thực sự cho điều trị nội mạch; tuy nhiên, tỉ lệ chữa khỏi chỉ với thuyên tắc mạch đơn độc tương đối thấp (~ 10-20%), ngoại trừ AVF màng mềm dòng chảy cao hoặc các tổn thương nhỏ. Bảng 2 tóm tắt các đặc điểm cấu trúc mạch máu này có thể ít tuân thủ cho điều trị nội mạch và xạ phẫu. Xạ phẫu có tỉ lệ chữa lành cao với tỉ lệ biến chứng tương đối thấp. Tuy nhiên, giới hạn chủ yếu của nó là xạ chậm có tác dụng, có thể đến 2 năm trước khi thấy AVM co lại. Vì vậy, xạ phẫu không thích hợp lắm để điều trị AVM não có các yếu tố nguy cơ trên chụp mạch đối với xuất huyết trong tương lai. Các tổn thương có thể tích trên 12ml liên quan với tỉ lệ chữa lành thấp hơn và tỉ lệ biến chứng cao hơn. Vì hiệu ứng tia xạ, xạ phẫu cần phải lưu ý khi sử dụng ở trẻ em. Điều trị bảo tồn thường được dùng khi nguy cơ do điều trị quá cao, như các AVM não lớn hoặc ở các bệnh nhân không có triệu chứng mà tin chắc là có nguy cơ xuất huyết thấp. Trong trường hợp AVM não lớn liên quan với một hoặc nhiều hơn các yếu tố nguy cơ đã đề cập trên, việc thuyên tắc mạch một phần hướng đến mục tiêu đã được chứng minh là có ích trong việc ngăn ngừa xuất huyết trong tương lai.
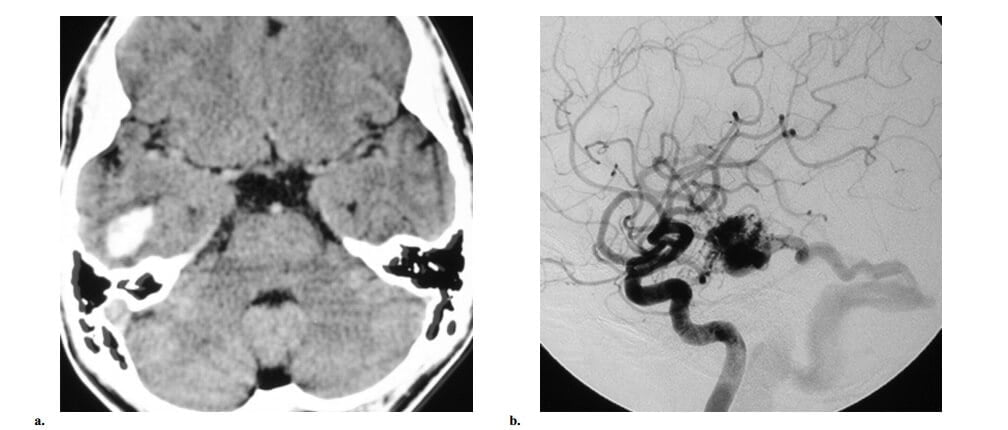
Hình 14: AVM não thái dương Spetzler- Martin grade 1 ở bé trai 15 tuổi có đă đầu đột ngột sau đó động kinh. (a) Axial CT thấy tổn thương tăng đậm độ nhỏ ở thùy thái dương phải, phù hợp với máu tụ trong nhu mô nhỏ. (b) Chụp động mạch cảnh trong phải thế nghiêng thấy một SVM nhỏ (<3cm) được cấp máu chủ yếu bởi nhánh thái dương của động mạch não giữa phải, với dẫn lưu nông vào tĩnh mạch Labbe phải.
Bảng 2. Các đặc điểm cấu trúc mạch máu với các nguy cơ liên quan trên điều trị nội mạch hoặc xạ phẫu đối với AVM não
TÓM LẠI
Chúng tôi đã nêu lên các đặc điểm hình ảnh học của AVM kinh điển cũng như các tổn thương mạch máu có thể giống AVM. Vì bệnh sử tự nhiên và các lựa chọn điều trị khác nhau theo các kiểu giống nhau này, điều quan trọng là các bác sĩ X quang phải phân biệt được chúng với các AVM não điển hình. Ngoài ra, chúng tôi cũng bàn luận đến các câu hỏi quan trọng nhất để trả lời được khi bác sĩ X quang gặp AVM não, gồm có hay không có các yếu tố nguy cơ xuất huyết hoặc các khiếm khyết thần kinh không xuất huyết. Chúng tôi cũng nêu lên các đặc điểm hình ảnh có thể giúp dự báo các nguy cơ liên quan với mỗi lựa chọn điều trị, vì vậy giúp bác sĩ lâm sàng đưa ra quyết định điều trị cho các tổn thương này.
- [Song ngữ Y khoa] Hình ảnh học dị dạng động tĩnh mạch não
- Cập nhật thuật ngữ, chẩn đoán, điều trị u máu và dị dạng mạch máu
- Hội chứng Seckel ở cậu bé tí hon K’rể và vai trò của siêu âm tiền sản
Trang web đang upload liên tục các video bài giảng và tài liệu chẩn đoán hình ảnh. Để nhận được thông báo về các bài viết mới nhất, vui lòng đăng ký tại Form nhận bản tin và theo dõi tại kênh Youtube















