Bài viết trong series DẤU HIỆU CHẨN ĐOÁN HÌNH ẢNH trình bày các dấu hiệu hình ảnh gợi ý hoặc đặc hiệu trên XQ, CT, MRI, Siêu âm.
Tiêu đề: Cập nhật chẩn đoán nốt mờ đơn độc tại phổi
Tác giả: Đào Ngọc Bằng*; Tạ Bá Thắng*; Đỗ Quyết**
Nguồn: Tạp chí Y – Dược học Quân sự, Số 7 (2019)
(*) Bệnh viện Quân y 103. (**) Học viện Quân y.
Tóm tắt
Một nốt mờ đơn độc tại phổi là một vấn đề thường gặp trong thực hành lâm sàng chuyên khoa hô hấp, được định nghĩa là một tổn thương đơn độc dạng tròn trên hình ảnh X quang phổi, với kích thước nốt ≤ 30 mm, xung quanh là nhu mô phổi lành, không liên quan đến xẹp phổi, hạch to trung thất hoặc tràn dịch màng phổi. Mục tiêu của chẩn đoán và xử trí kịp thời đưa vào phẫu thuật tất cả các bệnh nhân có nốt ác tính có thể phẫu thuật được, tránh phẫu thuật cắt phổi không cần thiết cho bệnh nhân có khối u lành tính. Trong thực tế, nguyên nhân nốt mờ tròn đơn độc có thể là lành tính hoặc ác tính. Để chẩn đoán nguyên nhân của các nốt mờ tròn đơn độc có thể sử dụng nhiều biện pháp, bao gồm: lâm sàng, đặc điểm X quang, sinh thiết lỏng, nội soi phế quản, sinh thiết hút dưới hướng dẫn của cắt lớp vi tính và phẫu thuật. Mỗi phương pháp đều có hiệu quả riêng trong chẩn đoán sớm nguyên nhân và đều có ý nghĩa cao. Dựa trên các kết quả chẩn đoán, bác sỹ có thể quyết định chiến lược xử trí bệnh.
Từ khóa: Nốt mờ đơn độc tại phổi; Chẩn đoán.
Nguyên nhân và tỷ lệ nốt mờ đơn độc tại phổi
Một nốt mờ đơn độc tại phổi được định nghĩa là một tổn thương đơn độc dạng tròn trên hình ảnh X quang phổi, với kích thước nốt ≤ 30 mm, xung quanh là nhu mô phổi lành, không liên quan đến xẹp phổi, hạch to trung thất hoặc tràn dịch màng phổi [1]. Nguyên nhân của nốt mờ tròn đơn độc tại phổi được phân làm 2 loại: lành tính và ác tính (Bảng 1). Tỷ lệ ước tính của mỗi nguyên nhân khác nhau ở các quần thể khác nhau. Ngay cả trong nghiên cứu quần thể những người hút thuốc lá-những người có nguy cơ mắc ung thư phổi cao, tỷ lệ nốt ác tính cũng thấp. Trong số 12.029 nốt mờ tròn được nghiên cứu tại Canada, chỉ 144 nốt (1%) là ác tính [2]
Đặc điểm của mỗi nguyên nhân rất khác nhau, bao gồm biểu hiện lâm sàng và thay đổi cận lâm sàng. Tùy theo đặc điểm của nốt mờ, bác sỹ có thể áp dụng các biện pháp phù hợp để chẩn đoán và xử trí.
Bảng 1: Chẩn đoán phân biệt các nốt mờ tròn đơn độc tại phổi [2]
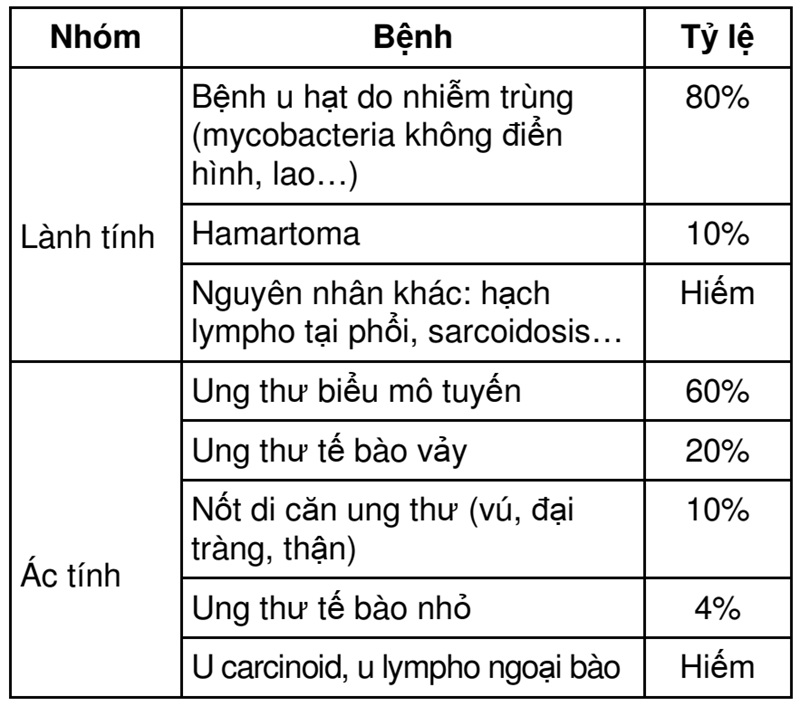
Chẩn đoán nốt mờ tròn đơn độc tại phổi
1. Đặc điểm các yếu tố nguy cơ
Khả năng ác tính được đánh giá bằng lâm sàng hoặc bằng yếu tố dự đoán, chia làm 3 nhóm: khả năng rất thấp (< 5%), khả năng thấp/trung bình (5 – 65%) và khả năng cao (> 65%). Những yếu tố được dùng để đánh giá thường xuyên nhất bao gồm 6 yếu tố tiên đoán độc lập: tiền sử hút thuốc, tuổi, tiền sử mắc các bệnh ung thư cơ quan khác > 5 năm trước khi phát hiện nốt mờ tròn tại phổi, đường kính nốt mờ, có tua gai và vị trí tại thuỳ trên của phổi. Có thể tính nguy cơ online tại trang web: http://reference.medscape.com/calculator/ solitary-pulmonary-nodule-risk [3].
Bảng 2: Cách tính khả năng ác tính của nốt mờ tròn đơn độc tại phổi [3].
| Yếu tố dự đoán | Giá trị |
|---|---|
| Tuổi | Tuổi bệnh nhân tính bằng năm |
| Tiền sử ung thư | 1: nếu có tiền sử mắc các bệnh ung thư cơ quan khác > 5 năm trước khi phát hiện nốt mờ tròn tại phổi (còn lại = 0) |
| Đường kính | Đường kính nốt mờ đo bằng mm |
| Vị trí | 1: nếu vị trí nốt mờ tại thuỳ trên của phổi (còn lại = 0) |
| Tiền sử hút thuốc | 1: nếu bệnh nhân hiện tại hoặc có tiền sử hút thuốc (còn lại = 0) |
| Có tua gai | 1: nếu nốt mờ có tua, gai (còn lại = 0) |
2. Đặc điểm X quang và PET/CT
Phần lớn các nốt mờ tại phổi được phát hiện trên hình ảnh CT-scan. Mặc dù một số nốt mờ được phát hiện trên X quang phổi, hình ảnh CT-scan phản ánh chi tiết những đặc điểm đặc hiệu của nốt mờ. Điểm đặc biệt quan trọng là CT-scan có thể đánh giá thay đổi về kích thước và tỷ lệ thay đổi theo thời gian bằng cách so sánh với những hình ảnh trước đó. Nhiều nghiên cứu đã chứng minh kích thước tăng lên có mối liên quan đến khả năng ác tính: kích thước nốt mờ < 5 mm, khả năng ác tính < 1%, kích thước nốt mờ 5 – 9 mm, khả năng ác tính từ 2 – 6%, kích thước nốt mờ 10 – 20 mm, khả năng ác tính 18%, kích thước nốt mờ ≥ 20 mm, khả năng ác tính > 50%. Những dấu hiệu phát triển trên phim chụp theo chuỗi có giá trị cao trong chẩn đoán ác tính. Tỷ lệ phát triển của nốt mờ cũng được sử dụng để đánh giá độ ác tính, phần lớn khối u ác tính có thời gian tăng gấp đôi về thể tích trong khoảng 20 – 400 ngày. Một nốt mờ thuần nhất không thay đổi trên 2 năm được coi là lành tính, trong khi với nốt mờ không thuần nhất trên 3 năm. Tỷ trọng của nốt mờ trên hình ảnh CT-scan có thể đặc trưng cho tính thuần nhất hoặc không thuần nhất. Không thuần nhất chia thành không thuần nhất hoàn toàn và không thuần nhất một phần. Mặc dù các tổn thương ác tính thường thuần nhất, tổn thương không thuần nhất cũng có thể là ác tính [4, 6].
Nên sử dụng CT-scan liều thấp để theo dõi các nốt mờ tròn tại phổi. Kỹ thuật này giảm liều chiếu so với phương pháp chụp CT-scan thông thường.
Hướng dẫn của National Comprehensive Cancer Network (NCCM) đề xuất các điểm cut-off khác nhau về kích thước, thời gian theo dõi và giám sát tuỳ thuộc vào xuất hiện của nốt mờ, thuần nhất hay không thuần nhất… Theo đề xuất của Fleishner (2017), các phương pháp theo dõi đa dạng, phụ thuộc vào nốt mờ thuần nhất hay không thuần nhất. Hướng dẫn của American College of Clinical Pharmacy (ACCP) đề xuất biện pháp tương tự, các phương pháp theo dõi phụ thuộc vào xuất hiện nốt mờ, kích thước và nguy cơ hoặc khả năng ác tính [3]. Nếu nốt mờ có nguy cơ cao nghĩ đến ác tính, sinh thiết không phẫu thuật hoặc cắt thuỳ phổi khi nốt mờ phát triển thành nốt thuần nhất. Phần lớn các hướng dẫn đề xuất sinh thiết không phẫu thuật hoặc cắt thuỳ phổi khi nốt mờ phát triển thành nốt thuần nhất. British Thoracic Society (BTS) đề xuất cắt thuỳ phổi khi nốt mờ phát triển có đường kính 2 mm [5, 6].
PET/CT: nhiều nghiên cứu đã chứng minh độ nhạy và độ đặc hiệu của PET/CT đối với chẩn đoán tổn thương ác tính lên tới 87% và 83%. Tuy nhiên, PET/CT cũng có những thiếu sót. Đầu tiên, PET không nhạy với các nốt có đường kính < 8 – 10 mm. Những BN ung thư biểu mô tuyến tại chỗ, ung thư biểu mô tuyến carcinoid và nhày, PET có thể cho kết quả âm tính giả. Kết quả dương tính giả có thể gặp ở BN có phản ứng viêm (hạch trong sarcoidosis hoặc thấp) hoặc có trạng thái nhiễm trùng (nhiễm nấm hoặc mycobacteria không điển hình) [5, 6].
Bảng 3: Đặc điểm X quang định hướng lành tính hay ác tính của nốt mờ tròn đơn độc [4].
| Đặc điểm X quang | Khả năng nốt lành tính | Khả năng nốt ác tính |
|---|---|---|
| Bờ | Đều | Không đều, có gai |
| Vôi hoá | Đồng tâm, trung tâm hoặc giống bỏng ngô | Thường không có vôi hoá hoặc vôi hoá lệch tâm |
| Tỷ trọng | Đồng nhất | Không đồng nhất |
| Thời gian tăng gấp đôi thể tích | < 1 tháng hoặc > 1 năm | 1 tháng đến 1 năm |
| Kích thước | < 5 mm | 10 mm |
Bảng 4: Tổng hợp biện pháp xử trí nốt mờ tròn đơn độc theo hướng dẫn ACCP [6].
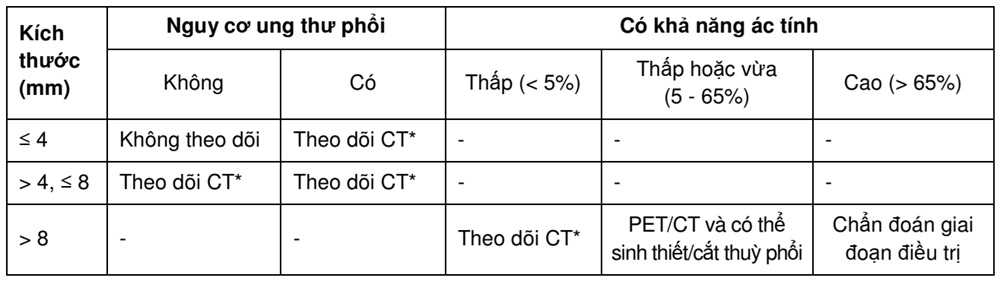
(*: Thời gian và thời hạn theo dõi CT phụ thuộc vào kích thước và xuất hiện nốt mờ, ACCP: American College of Clinical Pharmacy)
Bảng 5: Tổng hợp biện pháp xử trí nốt mờ tròn đơn độc theo hướng dẫn của Tổ chức Fleischner 2017 [5].

(*: Thời gian và thời hạn theo dõi CT phụ thuộc vào kích thước và xuất hiện nốt mờ)
- Lung-RADS v2022: Đánh giá phân loại và khuyến cáo quản lý
- Fleischner Society 2017: Hướng dẫn quản lý nốt phổi phát hiện tình cờ trên CT
- Tài liệu Hội nghị Chẩn đoán hình ảnh TP. Hồ Chí Minh mở rộng 2025
3. Sinh thiết lỏng
Sinh thiết lỏng là phân tích các dịch thể sinh học, đặc biệt là máu để phát hiện và định lượng dấu ấn ung thư, đây là phương pháp nên làm sớm và có giá trị trong chẩn đoán, tiên lượng ung thư. Không như sinh thiết mô thông thường, sinh thiết lỏng là một biện pháp không xâm nhập, an toàn, dễ thực hiện và không bị ảnh hưởng bởi kỹ năng. Đáng chú ý, một số dấu ấn ung thư được thực hiện với chi phí thấp, giúp sinh thiết lỏng khả thi trong xác định giai đoạn sớm của ung thư phổi. Hiện nay, nhiều loại dấu ấn ung thư có sẵn cho sinh thiết lỏng, bao gồm: các kháng nguyên liên quan khối u (tumor-associated antigens-TAAs), kháng thể liên quan đến khối u (tumorassociated autoantibodies-TAAbs), tế bào khối u lưu hành (circulating tumor cellsCTCs), ADN khối u lưu hành (circulating tumor DNA-ctDNA), microARN (miRNA), exosomes…. Các dấu ấn TAA có thể phát hiện trong dịch thể như carcinoembryonic antigen (CEA), carbohydrate antigen (CA) 125, CA199, neuron specific enolase (NSE), cytokeratin 19 fragment 21-1 (Cyfra 21-1) và carcinoma tế bào vảy (SCC) rất khó được sử dụng trong chẩn đoán sớm ung thư vì độ nhạy và độ đặc hiệu thấp. Tuy nhiên, các kháng nguyên liên quan khối u, kháng thể trong huyết thanh chống lại kháng nguyên tự thân có thể liên quan đến yếu tố thuận lợi trong chẩn đoán ung thư phổi sớm. Điều đó được giải thích, về mặt lý thuyết gồm: giám sát miễn dịch xảy ra ở pha sớm của quá trình chỉnh sửa miễn dịch ung thư, do đó các tự kháng thể có thể được phát hiện trong giai đoạn sớm của ung thư phổi. Các dấu ấn TAA có thể hiện diện ở nồng độ cao ngay cả khi khối lượng khối u thấp và ổn định trong máu. Các CTC là tế bào ung thư được tách trực tiếp từ khối u nguyên phát và/hoặc vị trí di căn, trôi dạt theo dòng tuần hoàn, có thể tập trung thành cụm hoặc đơn lẻ. Những tế bào ung thư này thường trải qua giai đoạn chuyển đổi trung biểu mô (EMT), xâm lấn và vận động sau khi tách khỏi biểu mô. Chúng có thể di chuyển vào lòng mạch bằng cách vượt qua thành mạch tới nơi chúng thường tập trung, trở thành CTC xâm lấn vào cơ quan xa và sinh sôi phát triển. Cho đến nay, các phương pháp ứng dụng trên lâm sàng để phát hiện CTC còn đang trong quá trình nghiên cứu. CT-ADN là các đoạn ADN không có tế bào đổ vào máu, do các tế bào khối u bị hoại tử, apoptotic hoặc tiết chủ động. Nó đặc hiệu cho khối u và cung cấp đặc điểm về mặt phân tử ADN của tế bào khối u và đột biến đặc trưng. Phân tích định tính và định lượng về đặc điểm sinh học của CT-ADN cho phép đánh giá chẩn đoán và tiên lượng. Một số nguồn dấu ấn ung thư từ sinh thiết lỏng có thể thực hiện để chẩn đoán sớm ung thư phổi, như exosome, MiRNA… [7].
4. Nội soi phế quản
Nội soi phế quản ảo (VB), nội soi phế quản dưới hướng dẫn từ (ENB), siêu nhỏ (UM), nội soi siêu âm phế quản toả tia (RP-EBUS) và ống soi siêu nhỏ được ứng dụng trong nội soi phế quản [9].
- Nội soi phế quản ống mềm truyền thống: nhiều nghiên cứu chứng minh phương pháp này có độ nhạy thấp đối với tổn thương < 2 cm, đặc biệt khi tổn thương ở ngoại vi [9].
- Nội soi ảo và nội soi ảo dẫn đường: nội soi ảo sử dụng CT không tương phản của ngực để xác định hình ảnh không gian ba chiều của đường thở, do đó có thể mô phỏng gần giống với đường thở thực tế. Việc lựa chọn nhánh phế quản tới tổn thương có thể là một sai sót chính trong tiếp cận tổn thương ngoại vi, nội soi ảo rất hữu ích trong chọn đường thở thích hợp. Nội soi phế quản ảo dẫn đường liên quan đến điều hướng đi tới tổn thương ngoại vi dựa trên đường thở dẫn tới tổn thương do nội soi ảo và các điểm nội soi ảo và nội soi thực tế xếp chồng lên nhau [9].
- Nội soi ống siêu nhỏ: những ống nội soi nhỏ với đường kính 2,8 – 3,5 mm được coi là siêu nhỏ dù không có định nghĩa chính thức. Kích thước nhỏ của ống nội soi cho phép ống cơ động tốt hơn và quan sát phế quản sâu hơn, từ thứ 6 đến thứ 8. Ống nội soi siêu nhỏ thường được kết hợp với kỹ thuật hình ảnh dẫn đường để tiếp cận với tổn thương ngoại vi tốt hơn [9].
- Nội soi phế quản siêu âm đầu dò tỏa tia: sử dụng tần số 20 MHz với đầu dò có thể xoay 3600 vuông góc với hướng siêu âm và cho hình ảnh có độ phân giải cao về cấu trúc đường thở. Đầu dò siêu âm có thể đưa trực tiếp qua kênh sinh thiết của ống nội soi, nhờ bộ dẫn đường hoặc qua kênh hoạt động mở rộng của hệ thống điều hướng điện từ để xác định vị trí phù hợp của khu vực cần đánh giá. Khi tổn thương được xác định, bộ dẫn đường cố định vị trí, rút đầu dò siêu âm và dụng cụ lấy bệnh phẩm tổn thương đưa qua bộ dẫn đường. Dựa trên nhiều nghiên cứu có hệ thống, độ nhạy chung của nội soi phế quản siêu âm đầu dò tỏa tia trong chẩn đoàn tổn thương ngoại vị khoảng 70% tùy từng nghiên cứu, mặc dù không có sự đồng nhất về đặc điểm của nốt mờ và công nghệ hình ảnh hướng dẫn bổ sung. Hạn chế chính của kỹ thuật là phụ thuộc vào thủ thuật viên nội soi [9].
- Nội soi phế quản điều hướng điện từ: hệ thống nội soi phế quản điều hướng điện từ làm việc tương tự với hệ thống GPRS. Phương pháp này đòi hỏi CT-scan có độ phân giải cao để đánh giá hình ảnh cây phế quản ảo. Chụp CT được thực hiện trước khi làm kỹ thuật này. Đánh giá tổn thương theo nhiều hướng khác nhau và đánh dấu từng mục tiêu. Xác định đường phế quản đi tới tổn thương và đánh dấu bằng đường phế quản ảo. Nghiên cứu về kỹ thuật này thường nhỏ, đơn trung tâm và không ngẫu nhiên, với hiệu quả chẩn đoán đạt 63 – 85%. Những yếu tố liên quan đến độ nhạy cao là kích thước nốt mờ lớn, sự có mặt của dấu hiệu phế quản, hình ảnh nốt trên nội soi siêu âm phế quản… [9].
5. Chọc hút kim nhỏ dưới hướng dẫn CT-scan
Phương pháp này thường được thực hiện trong thực hành lâm sàng, đặc biệt đối với nốt mờ gần thành ngực. Độ chính xác của kỹ thuật phụ thuộc nhiều vào kỹ năng của thủ thuật viên trong lựa chọn vị trí và chọc u lấy bệnh phẩm, cũng như trình độ đọc giải phẫu bệnh lý, là những yếu tố có thể ảnh hưởng nhất định đến kết quả. Cùng với vai trò sàng lọc ung thư phổi của CT, việc ứng dụng rộng rãi CT với độ phân giải cao, số lượng nốt mờ tròn đơn độc được chẩn đoán ngày càng tăng. Trong những năm gần đây, một loại nốt mờ quan trọng đang tăng dần, được gọi là nốt mờ dưới 1 cm, đặc biệt với nốt có kích thước < 8 mm. Mặc dù phần lớn các nốt này là lành tính, nên làm giải phẫu bệnh nốt mờ cho BN có tiền sử ung thư, ngay cả khi các nốt này nhỏ và ở ngoại vi. Đây là phương pháp xâm lấn tối thiểu, độ nhạy chẩn đoán cao, ít thương tổn và giá thành thấp. Vì vậy, thường được sử dụng rộng rãi trong chẩn đoán nốt mờ. Chẩn đoán nốt mờ nhỏ bằng chọc hút kim nhỏ dưới hướng dẫn CT có các đặc điểm sau:
- Phạm vi ứng dụng rộng rãi: ngoại trừ tổn thương ở trung tâm, tỷ lệ chẩn đoán của nội soi phế quản với tổn thương ngoại vi và lan tỏa rất thấp, trong khi kỹ thuật này áp dụng cả với tổn thương trung tâm, ngoại vi và lan tỏa, không sát mạch máu.
- Độ chính xác cao: kể cả tổn thương có kích thước 0,5 – 1 cm, biện pháp này cũng áp dụng thành công dưới hướng dẫn của CT.
- Độ chính xác trong chẩn đoán cao: đây là một kỹ thuật hữu ích. Tuy nhiên, độ chính xác của chẩn đoán phụ thuộc vào kích thước và vị trí của tổn thương, cũng như kỹ thuật hướng dẫn, giảm từ trên 90% xuống 25% khi nốt ác tính nhỏ (< 1 cm) và 70% khi tổn thương lành tính.
- Độ an toàn cao: mặc dù kỹ thuật này là một phương pháp an toàn và đáng tin cậy nhưng vẫn là một kỹ thuật xâm nhập và có tai biến. Biến chứng chủ yếu tràn khí màng phổi và chảy máu. Theo các nghiên cứu, tỷ lệ tràn khí màng phổi khoảng 10 – 40%, trong khi tỷ lệ tổn thương phổi khoảng 26 – 33% [10].
6. Phẫu thuật
Trường hợp nốt có khả năng ác tính cao (60 – 70%), phẫu thuật nội soi lồng ngực được áp dụng để chẩn đoán, xa hơn nữa để điều trị. Với những tổn thương lành tính từ sinh thiết tức thì, chỉ cần cắt thùy phổi hình chêm. Với tổn thương ác tính, cắt thùy phổi kết hợp nạo vét hạch khu vực [10].
Tài liệu tham khảo
- Zhou Z, Zhan P, Jin J et al. The imaging of small pulmonary nodules. Translational Lung Cancer Research. 2017, 6 (1), pp.62-67.
- Kikano G.E, Fabien A. and Schilz R. Evaluation of the solitary pulmonary nodule. American Family Physician. 2015, 92 (12), pp.1084-1092.
- NCCN Lung Cancer Screening Panel Members. Lung cancer screening, Version 3.2018. Journal of the National Comprehensive Cancer Network. 2018, 16 (4), pp.412-441.
- Gould M.K, Donigton J, Lynch W.R et al. Evaluation of individuals with pulmonary nodules: When is it lung cancer?. Chest. 2013, 143 (5), pp.93-120.
- MacMahon H, Naidich D.P, Goo J.M et al. Guidelines for management of incidental pulmonary nodules detected on CT images: From the Fleischner Society. Radiology. 2017, 284 (1).
- Ito M, Myiata Y and Okada M. Management pathways for solitary pulmonary nodules. Journal of Thoracic Disease. 2018, 10 (7), pp.860-866.
- Liang W, Zhao Y, Hoang W. Liquid biopsy for early stage lung cancer. Journal of Thoracic Disease. 2018, 10 (7), pp.876-881.
- Castro-Giner F, Gkoutela S, Donato C et al. Cancer diagnosis using a liquid biopsy: Challenges and expections. Diagnostics (Basel). 2018, 8 (2), p.31.
- Dhillon S.S, Harris K. Bronchoscopy for the diagnosis of peripheral lung lesions. Journal of Thoracic Disease. 2017, 9 (10), pp.1047-1058.
- Xu C, Hao K, Song Y et al. Early diagnosis of solitary pulmonary nodules. Journal of Thoracic Disease. 2013, 5 (6), pp.830-840.
Trang web đang upload liên tục các video bài giảng và tài liệu chẩn đoán hình ảnh. Để nhận thông báo về các bài viết mới nhất, vui lòng đăng ký Nhận bài viết mới và theo dõi Kênh Youtube















